
Exploatați puterea insulinei

Cum structurați dieta pentru a construi mușchi fără să îngrășați sau să pierdeți grăsimea corporală în timp ce câștigați sau mențineți mușchi? Există o mulțime de strategii disponibile care urmăresc să atingă aceste obiective, dar până acum recenziile au fost mixte. Din păcate, nu există o abordare de tăiere a cookie-urilor, care să funcționeze pentru fiecare metabolism.
Vestea bună este că toate efectiv strategiile de dietă au un lucru în comun: folosesc cel mai bine insulina.
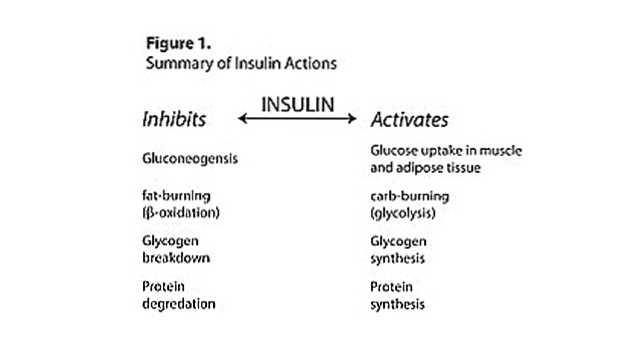
Insulina este un puternic inductor al absorbției de aminoacizi și al sintezei proteinelor, făcându-l cel mai „hormon anabolic” din organism. Dar insulina are și o latură mai întunecată, ca un puternic inductor al depozitării grăsimilor.
Prima lege a termodinamicii
Prima lege a termodinamicii afirmă că „energia din cadrul unui sistem închis rămâne constantă.”Aceasta înseamnă că energia poate fi transformată (schimbată într-o formă sau alta), dar nu poate fi creată sau distrusă. Pentru a slăbi, trebuie să consumi mai puțină energie decât arzi. Pentru a câștiga în greutate, trebuie să luați mai multă energie decât ardeți. Mănâncă prea mult și vei îngrășa, indiferent de unde provin caloriile.
Este atat de simplu. Nu există o combinație „magică” de macronutrienți, micronutrienți, momentele mesei, suplimente sau chiar medicamente pentru a evita acest lucru. Dacă sunteți genul care are nevoie de cineva sau de ceva de vină, începeți cu evoluția, universul sau GOP.
Cu toate acestea, o calorie este nu doar o calorie pe termen lung. Diferenți macronutrienți produc diferite efecte pe termen lung hormonal și metabolic.
Partiționarea nutrienților: importanța macronutrienților
Deși nu putem modifica legile universului, avem unii care spun cum se folosește energia din alimentele pe care le consumăm. Partiționarea nutrienților determină ce face organismul cu energia din dietă. Caloriile sunt fie arse și utilizate pentru energie imediată, fie stocate pentru considerații viitoare. Având în vedere druthers noștri, toată energia noastră suplimentară ar fi folosită pentru a alimenta creșterea musculară nouă și a acumula depozite de glicogen muscular, nu stocate ca grăsime corporală. La urma urmei, ca sportivi, vrem să fim slabi, musculoși și plini, nu grași și plati.
Cu toate acestea, spre deosebire de prima lege a termodinamicii, macronutrienții contează pentru împărțirea nutrienților. Deci, cum maximizăm depozitele de glicogen muscular și minimizăm grăsimea corporală, în timp ce câștigăm sau menținem mușchiul?
Partiționarea nutrienților este reglementată de multe țesuturi, o acțiune coordonată a ficatului, intestinului, creierului / SNC, țesutului adipos și mușchilor, împreună cu o simfonie de hormoni, mesageri secundari și canale ionice. Oamenii de știință nici măcar nu sunt siguri exact cum funcționează totul. Împărțirea nutrienților devine disfuncțională la obezi și diabetici, care sunt, de asemenea, rezistenți la insulină. Aceasta nu este o coincidență; insulina joacă un rol imens în împărțirea nutrienților. Cu cât sunteți mai „sensibil” la insulină, cu atât mai mulți nutrienți sunt împărțiți în favoarea dumneavoastră.
Curs accidental în semnalizarea insulinei
- Toți carbohidrații din dietă sunt descompuși în glucoză în intestinul subțire, care este apoi absorbit în fluxul sanguin. Aceasta va fi utilizată fie ca sursă de energie imediată pentru sinteza ATP, fie va fi stocată, conform instrucțiunilor insulinei.
- Glucoza este stocată ca glicogen în ficat și în țesutul muscular sau este transformată în trigliceride și stocată ca grăsime corporală.
Evident, dorim să maximizăm stocarea glicogenului muscular și sinteza proteinelor în țesutul muscular, reducând în același timp creșterea grăsimilor. Cu toate acestea, credința populară că aportul de carbohidrați peste un anumit punct „se varsă” în celulele adipoase este nu corect. Insulina nu este selectivă. Stimulează în mod constant celulele grase pentru a prelua glucoza, unde este transformată în glicerol sau acizi grași, ambii fiind necesari pentru a forma trigliceride care sunt stocate ca grăsime corporală.
Asta înseamnă că suntem mereu stocarea grăsimii corporale după masă, deși acest lucru nu este atât de rău pe cât pare. În condiții normale, mușchii reprezintă 85-90% din eliminarea glucozei stimulată de insulină, în timp ce grăsimile reprezintă doar 5-15%.
Dar mâncați prea mulți carbohidrați (sau un fel greșit), iar lucrurile se pot schimba. Glucoza va fi depusă numai în țesutul muscular și hepatic până când depozitele de glicogen sunt pline, restul acestei energii în exces va fi transformat în acizi grași și stocat ca trigliceride în țesutul adipos.
Introduceți rezistența la insulină
Aici intervine rezistența la insulină. Consultați diagrama de mai jos. Observați receptorul de insulină de pe membrana celulară. Când insulina intră în contact cu receptorul, acesta începe o serie de evenimente care duc în cele din urmă la translocarea GLUT 4 către membrana celulară.
Insulina este doar mesagerul. Acțiunea reală are loc cu GLUT4, care permite glucozei să pătrundă în celulă.
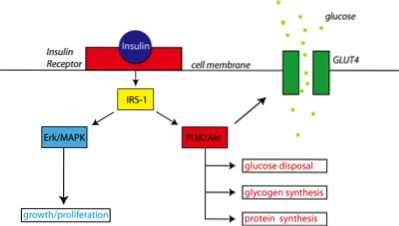
Pentru cei care sunt rezistenți la insulină, parcă primesc „bătaia la ușă” (receptorul de insulină pe membrana celulară), dar nimeni nu răspunde. Nu există un semnal „go” dat proteinelor GLUT4. Acum, împărțirea nutrienților devine dificilă. În acest caz, va exista o translocație GLUT4 redusă sau deloc, iar glucoza și alți nutrienți nu pot intra în celulă. Aceasta este o problemă, deoarece glucoza la niveluri ridicate în sânge este toxică, motiv pentru care organismul este pregătit dispune de glucoză pe măsură ce pătrunde în fluxul sanguin.
Deci, ce se întâmplă când bateți la o ușă și nimeni nu răspunde? Ei bine, bateți mai tare. Așa se întâmplă cu rezistența la insulină; insulina este eliberată din ce în ce mai mult pentru a activa GLUT4.
Modul în care rezistența la insulină cauzează creșterea grăsimilor
Cu cât răspunsul la insulină este mai mare, cu atât mașinile de semnalizare a insulinei vor deveni mai rezistente la efectele insulinei, în special în țesutul muscular. Această mașină de semnalizare a insulinei desensibilizează acut chiar și la persoanele sănătoase.
Mănâncă prea mulți sau un tip greșit de carbohidrați la momentul nepotrivit și vor fi transformați în grăsimi printr-un proces numit denovo lipogeneza. Acest lucru este prin proiectare, deoarece avem doar capacitatea de a stoca atât de mult glicogen. Când aceste depozite sunt completate, sensibilitatea la insulină scade pentru a semnala că depozitele de glicogen sunt pline. Dar orice glucoză rămasă în fluxul sanguin trebuie încă eliminată.
Pentru a realiza acest lucru, se eliberează mai multă insulină, determinând excesul de glucoză să fie transformat în trigliceride prin denovo lipogeneza. Aceste trigliceride sunt apoi depozitate ca grăsime în țesutul adipos.
Îmbunătățirea sensibilității la insulină: o reîmprospătare
Acordați atenție tipului de carbohidrați și calendarului.
O recomandare slabă este să consumați 70% din carbohidrați în timpul fazei pre, intra și post antrenament. Celelalte 30% trebuie adăugate la micul dejun și / sau la a doua masă după antrenament. Dacă te antrenezi dimineața, atunci prânzul tău ar fi o alegere mai bună pentru aportul suplimentar de carbohidrați.
Aceasta nu este o linie directoare universală - toată lumea are nevoi diferite de carbohidrați în funcție de metabolismul lor, de tipul de antrenament și de suplimentele pe care le iau, cum ar fi Indigo-3G®, care pare să vă permită să ingerați mai mulți carbohidrați decât în mod obișnuit. Este o regulă generală eficientă care face o treabă bună de a face oamenii mai slabi fără a compromite câștigurile în mușchi / țesut slab.
Deci, dacă consumați 300 de grame de carbohidrați în zilele în care vă antrenați extrem de greu, consumați 200 de grame în timpul fazei pre, intra și post antrenament.
De exemplu:
- Pre-antrenament: 1 cană de ovăz și 1 cană de afine. (54 + 22 = 76 grame)
- Intra: 1 lingură de Plamza ™. (38 grame)
- Post: 8 uncii de cartof dulce. (56 grame)
- Total = 170 grame de carbohidrați
Celelalte 100 de grame aproximativ ar fi plasate în micul dejun (50 de grame) și a doua masă după antrenament. Structurarea aportului de carbohidrați în acest mod le oferă „scop” și asigură o mai bună repartizare a nutrienților.
Folosiți agenți de eliminare a glucozei.
Puteți conduce mai mulți nutrienți în mușchi utilizând insulină exogenă. Eu nu face susțineți această opțiune, deoarece pancreasul este un lucru teribil cu care să vă încurcați. Cu cât este mai puțin necesară insulina pentru a face treaba, cu atât vei fi mai slab!
Limitați aportul total de carbohidrați.
Excesiv dietele bogate în carbohidrați scad sensibilitatea la insulină. Relația dintre nivelurile de insulină și sensibilitatea la insulină este neliniară, ceea ce înseamnă că aportul ridicat de carbohidrați, chiar și în limitele normale de eliberare a insulinei, poate provoca o scădere semnificativă a sensibilității la insulină. Nivelurile crescute de insulină determină „blocarea” metabolismului în modul de ardere a carbohidraților prin activarea expresiei genelor pentru metabolismul carbohidraților și reglarea în jos a expresiei genelor pentru oxidarea grăsimilor.
O persoană medie are în jur de 350-400 de grame de rezerve de glicogen în țesutul muscular și încă 100 de grame în ficat. Dacă carbohidrații suplimentari nu sunt arși pentru energie imediată, sunt transformați în trigliceride și depozitați ca grăsime corporală.
Nu interpretați greșit acest lucru ca pe un „carbohidrați sunt un mesaj rău.”Din nou, exces carbohidrații sunt vinovații.
Îmbunătățirea partiției nutrienților prin combaterea rezistenței la insulină
Limitați inflamația. Ați auzit, fără îndoială, despre rapoartele omega-6 la omega-3 pentru sănătatea generală. Iată, de asemenea, ajută la combaterea rezistenței la insulină.
Inflamația are un efect negativ asupra sensibilității la insulină, deci controlul acesteia este o parte importantă a ecuației de împărțire a nutrienților. Inflamația cronică este un numitor comun pentru obezitate și diabetul de tip 2, deci dacă conectăm punctele, o sensibilitate slabă la insulină înseamnă că veți fi predispus să câștigați grăsimi și să împărțiți nutrienții mai puțin eficient.
Notă: Nivelul general al inflamației în organism este determinat de raportul dintre grăsimile omega-6 și omega-3 din membranele celulare.
Acizii grași polinesaturați Omega-6 și Omega-3 sunt precursori ai unor molecule de semnalizare puternice numite eicosanoizi care joacă un rol important în reglarea inflamației. Grăsimile omega-6 promovează formarea eicosanoidelor inflamatorii, în timp ce grăsimile omega-3 promovează versiunile antiinflamatoare. Asta da nu înseamnă că nu vrem nici unul dintre eicosanoizii inflamatori „răi”; sunt necesare pentru lucruri precum vindecarea rănilor. Din nou, revine la raport.
Corpul uman poate produce toți acizii grași de care are nevoie, cu excepția acidului linoleic (LA), a unei grăsimi omega-6 și a acidului α-linolenic (ALA), a unei grăsimi omega-3. Aceste grăsimi sunt esențiale și este esențial să le includem în dietă în raporturile corecte pentru a limita inflamația.
„Dieta occidentală” tipică determină supraproducția eicosanoidelor inflamatorii, rezultând inflamații cronice și sensibilitate redusă la insulină. Raportul „ideal” omega 6: 3 de 4: 1 optimizează sensibilitatea la insulină prin echilibrarea producției de prostaglandine pro și antiinflamatoare.
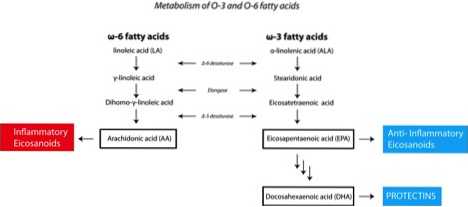
Notă. Doar 8-20% din ALA din organism este convertit în EPA, în timp ce conversia ALA în DHA este chiar mai mică, în jur de 0.5-9%. Acest lucru înseamnă că este greu să obții suficient EPA și DHA pentru a limita inflamația și pentru a atinge niveluri optime de sensibilitate la insulină numai prin consumul de ALA.
Vestea bună este că peștii grași precum somonul, păstrăvul și heringul sunt încărcați cu EPA și DHA. De asemenea, puteți spori EPA și DHA cu ulei de pește sau suplimente precum Flameout®.
Oamenii de știință au descoperit recent că răspunsul inflamator care determină rezistența la insulină și diabetul este legat de țesutul adipos. Până de curând, țesutul adipos era considerat a fi stocarea „pasivă” a energiei lipidice, dar știm acum că depozitele de grăsimi funcționează și pentru a controla sensibilitatea la insulină a întregului corp.
Oamenii de știință au început să analizeze mai îndeaproape țesutul adipos atunci când s-a constatat că supraexprimarea GLUT4 în adipocite a îmbunătățit de fapt sensibilitatea la insulină a întregului corp. Câțiva ani după aceea, s-a descoperit că eliminarea genei GLUT4 în mod specific în țesutul adipos a cauzat rezistență la insulină în mușchi și ficat, demonstrând că țesutul adipos afectează semnificativ modul în care funcționează insulina în restul corpului.
Grăsimea este într-adevăr un organ endocrin, secretând o serie de hormoni numiți „adipokine” care controlează sensibilitatea și inflamația la insulină a întregului corp.
Până în prezent au fost identificate peste 50 de adipokine diferite, care pot avea efecte pozitive sau negative asupra sensibilității la insulină. Adipokinele „bune”, inclusiv leptina și adiponectina, sunt agenți puternici de împărțire a nutrienților. Împreună, leptina și adiponectina cresc arderea grăsimilor, scad stocarea grăsimilor și cresc sensibilitatea la insulină.
Adipokinele „rele”, inclusiv rezistina, TNFα și alte citokine, cum ar fi IL-6, cresc rezistența la insulină prin creșterea inflamației. Din fericire, avem un cuvânt de spus cu privire la tipul și nivelul adipokinelor care sunt secretate din celulele adipoase. Grăsimile omega 3 EPA și DHA promovează producția de adipokine „bune”, care cresc sensibilitatea la insulină și optimizează partiția nutrienților.
EPA și DHA privind sensibilitatea la insulină și inflamație
- Reduceți inflamația prin promovarea formării de eicosanoizi antiinflamatori.
- Creșteți direct producția de „bune” adipokine adiponectină și leptină de către celulele adipoase.
- Creșteți sensibilitatea la insulină prin stimularea directă a unui receptor care limitează producția de inflamație și adipokine „rele” în țesutul adipos.
Următorul: Nu te stresa!
Faceți orice altceva bine și acesta vă poate obține în continuare. Stresul are un puternic efect negativ asupra sensibilității la insulină și a modului în care împărțim nutrienții. Cercetătorii au descoperit că sistemul nervos autonom (ANS) este, de asemenea, un maestru în reglarea semnalizării insulinei. ANS reglează funcțiile vitale involuntare, constând din sistemul nervos simpatic (SNS) și sistemul nervos parasimpatic (PNS).
SNS este mai frecvent cunoscut sub numele de „luptă sau fugă”. Răspunde la stres prin accelerarea ritmului cardiac, constrângerea vaselor de sânge, creșterea tensiunii arteriale și reducerea activității digestive; practic, tot ce ai nevoie pentru a lupta sau a fugi de pericol. PNS contracarează SNS prin inducerea unui răspuns de relaxare (tensiunea arterială și ritmul cardiac sunt reduse, activitatea digestivă este crescută etc.). Echilibrul general dintre activitatea PNS și SNS determină cât de multă insulină este eliberată și sensibilitatea la insulină.
- PNS scade consumul de energie și potențează efectele insulinei în țesuturile țintă prin creșterea sensibilității la insulină, activând absorbția glucozei și stocarea glicogenului.
- SNS crește consumul de energie, scade sensibilitatea la insulină și declanșează lipoliza în țesutul adipos. Efectul general al SNS este de a crește utilizarea grăsimilor pentru combustibil în timp ce se află în modul luptă sau zbor pentru a păstra glicogenul muscular.
Acest sistem ne-a servit bine în zilele noastre ancestrale. Atunci când se confruntă cu un tigru cu dinți de sabie sau cu o femeie din peșteră care mânuiește un club supărat, sistemul SNS a dat lovitura, pregătindu-ne să luptăm sau să fugim. Dacă am reușit să supraviețuim, activitatea ANS a revenit la normal odată cu stresul scăzut.
Dar astăzi, stresul tinde să fie cronic în loc de acut, cum ar fi termenele limită, impozitele, blocajele de trafic, soțiile furioase cu mături, etc. Acest lucru ne pune într-o stare constantă de stres, rezultând un dezechilibru între ramurile SNS și PNS ale sistemului nervos autonom.
Nivelurile cronice / ridicate de stres fac ca ANS să se dezechilibreze prin supraactivarea sistemului SNS. Acest lucru poate duce la rezistență la insulină, oboseală suprarenală, hipertensiune arterială și creșterea defalcării musculare.
Lăsat necontrolat, stresul poate fi un ucigaș. Nu putem afirma suficient importanța acestui lucru. Nivelurile ridicate de stres sunt otrăvitoare pentru un fizic excelent.
Optimizați semnalizarea insulinei prin echilibrarea activității PNS și SNS
- Nu vă faceți griji cu privire la lucrurile pe care nu le puteți controla.
- Dormi suficient.
- Evitați fraierii de viață. Știi cine sunt.
- Învață să te relaxezi. Relaxarea promovează activitatea ANS, crescând sensibilitatea la insulină (creșterea musculară, stocarea glicogenului, etc.).
- Antreneze din greu! Antrenamentul este tipul de stres acut pentru care am fost proiectați. O combinație de antrenament intens și odihnă menține sistemul nervos în starea corectă de echilibru pentru câștiguri musculare slabe.
Rezumând
În circumstanțe normale, sensibilitatea la insulină este controlată cu precizie pentru a menține punctul de echilibru numit homeostazie energetică. Ca sportivi, obiectivul nostru este de a conduce glucoza maximă în țesutul muscular și glucoza minimă în țesutul adipos. Acest lucru necesită o sensibilitate optimă la insulină, o problemă de împărțire a nutrienților.
Scopul împărțirii nutrienților este de a obține un echilibru în care substanțele nutritive sunt direcționate în principal către masa musculară și stocarea glicogenului, în timp ce pierde sau menține niveluri scăzute de grăsimi corporale. Acesta este un loc subtil, dar la fel cum corpul echilibrează nenumărați factori pentru a menține homeostazia energetică, eforturile noastre de împărțire a nutrienților trebuie să fie și „echilibrate”.
În condiții normale, sistemul se auto-reglează, dar urmând liniile directoare pe care le-am prezentat în acest articol, veți fi pe drumul spre o persoană mai slabă și mai musculară, mai sanatos fizic.
Toate cele bune,
Bill și John
Referințe
- Kahn BB. Lectie Lilly 1995. Transportul glucozei: pas esențial în acțiunea insulinei. Diabet 1996; 45: 1644-54.
- Kahn SE, Hull RL, Utzschneider KM. Mecanisme care leagă obezitatea de rezistența la insulină și diabetul de tip 2. Natura 2006; 444: 840-6.
- SchutzY. Conceptul de echilibru al grăsimilor la obezitatea umană revizuit cu o referire specială la lipogeneza de novo. Int J Obes Relat Metab Disord 2004; 28 Suppl 4: S3-S11.
- Schwarz JM, Linfoot P, Dare D, Aghajanian K. Lipogeneză hepatică de novo la subiecți normoinsulinemici și hiperinsulinemici care consumă diete izoenergetice bogate în grăsimi, cu conținut scăzut de carbohidrați și cu conținut scăzut de grăsimi, cu conținut ridicat de carbohidrați. Jurnalul American de Nutriție Clinică 2003; 77: 43-50.
- Parks EJ. Efectele carbohidraților dietetici asupra lipogenezei și relația lipogenezei cu concentrațiile de insulină și glucoză din sânge. Br J Nutr 2002; 87 Suppl 2: S247-S253.
- KoltermanOG, Greenfield M, Reaven GM, Saekow M, Olefsky JM. Efectul unei diete bogate în carbohidrați asupra legării insulinei de adipocite și asupra acțiunii insulinei in vivo la om. Diabet 1979; 28: 731-6.
- Roberts R, Bickerton AS, Fielding BA, Blaak EE, Wagenmakers AJ, Chong MF și colab. Reducerea oxidării grăsimilor dietetice după o dietă bogată în carbohidrați pe termen scurt. Am J Clin Nutr 2008; 87: 824-31.
- SemenkovichCF. Rezistența la insulină și ateroscleroza.J Clin Invest 2006; 116: 1813-22.
- Calder PC. n-3 acizi grași polinesaturați, inflamații și boli inflamatorii. Am J Clin Nutr 2006; 83: 1505S-19S.
- SerhanCN, Hong S, Gronert K, Colgan SP, Devchand PR, Mirick G și colab. Resolvine: o familie de produse bioactive din circuite de transformare a acizilor grași omega-3 inițiată prin tratamentul cu aspirină care contracarează semnalele proinflamatorii. J Exp Med 2002; 196: 1025-37.
- Schwab JM, Chiang N, Arita M, Serhan CN. Resolvin E1 și protectina D1 activează programele de rezoluție a inflamației. Natura 2007; 447: 869-74.
- SimopoulosAP. Importanța raportului dintre acizii grași esențiali omega-6 / omega-3: aspecte evolutive. World Rev Nutr Diet 2003; 92: 1-22.
- BurdgeGC. Metabolismul acidului alfa-linolenic la om. Prostaglandine Leukot Essent Fatty Acids 2006; 75: 161-8.
- DeFilippisAP, Sperling LS. Înțelegerea omega-3. Am Heart J 2006; 151: 564-70.
- WellenKE, Hotamisligil GS.Inflamație, stres și diabet. J Clin Invest 2005; 115: 1111-9.
- ShoelsonSE, Lee J, Goldfine AB. Inflamația și rezistența la insulină. J Clin Invest 2006; 116: 1793-801.
- Rosen ED, Spiegelman BM. Adipocitele ca reglatoare ale echilibrului energetic și ale homeostaziei glucozei. Natura 2006; 444: 847-53.
- GnudiL, Tozzo E, Shepherd PR, Bliss JL, Kahn BB. Supraexpresia la nivel ridicat a transportorului de glucoză-4 condus de un promotor specific adipos este menținută la șoarecii transgenici pe o dietă bogată în grăsimi, dar nu previne afectarea toleranței la glucoză. Endocrinologie 1995; 136: 995-1002.
- Abel ED, Peroni O, Kim JK, Kim YB, Boss O, Hadro E, și colab. Direcționarea selectivă a adipozei a genei GLUT4 afectează acțiunea insulinei în mușchi și ficat. Natura 2001; 409: 729-33.
- TrayhurnP. Rolul endocrin și de semnalizare a țesutului adipos: noi perspective asupra grăsimii. Acta Physiol Scand 2005; 184: 285-93.
- Havel PJ. Actualizare privind hormonii adipocitari: reglarea echilibrului energetic și a metabolismului carbohidraților / lipidelor. Diabet 2004; 53 Suppl 1: S143-S151.
- Wall R, Ross RP, Fitzgerald GF, Stanton C. Acizi grași din pești: potențialul antiinflamator al acizilor grași omega-3 cu lanț lung. Nutr Rev 2010; 68: 280-9.
- Murata M, Kaji H, Takahashi Y, Iida K, Mizuno I, Okimura Y și colab. Stimularea de către acizii eicosapentaenoici a expresiei mARN-ului leptinei și secreția acestuia în adipocite 3T3-L1 de șoarece in vitro. Biochem Biophys Res Commun 2000; 270: 343-8.
- Perez-Matute P, Marti A, Martinez JA, Fernandez-Otero MP, Stanhope KL, Havel PJ și colab. Acidul gras eicosapentaenoic crește secreția de leptină din adipocitele primare de șobolan cultivate: rolul metabolismului glucozei. Am J Physiol Regul Integr Comp Physiol 2005; 288: R1682-R1688.
- ItohM, Suganami T, Satoh N, Tanimoto-Koyama K, Yuan X, Tanaka M și colab. Creșterea secreției de adiponectină de acid eicosapentaenoic foarte purificat la modelele de rozătoare ale obezității și subiecților obezi umani. Arterioscler Thromb Vasc Biol 2007; 27: 1918-25.
- Oh DY, Talukdar S, Bae EJ, Imamura T, Morinaga H, Fan W, și colab. GPR120 este un receptor de acizi grași omega-3 care mediază efecte puternice antiinflamatoare și sensibilizante la insulină. Celula 2010; 142: 687-98.
- KreierF, Fliers E, Voshol PJ, Van Eden CG, Havekes LM, Kalsbeek A și colab. Inervație parasimpatică selectivă a implicațiilor funcționale ale grăsimii subcutanate și intra-abdominale. J Clin Invest 2002; 110: 1243-50.
- RobidouxJ, Martin TL, Collins S. Receptorii beta-adrenergici și reglarea cheltuielilor de energie: o aventură de familie. Annu Rev Pharmacol Toxicol 2004; 44: 297-323.
- Schwartz MW, Woods SC, Porte D, Jr., Seeley RJ, Baskin DG. Controlul sistemului nervos central al consumului de alimente. Nature 2000; 404: 661-71.



Nimeni nu a comentat acest articol încă.